 BUSCAR
BUSCAR
 ÍNDICE
ÍNDICE
CIRCULAR EXTERNA 00000005 DE 2025
(febrero 18)
Diario Oficial No. 53.035 de 19 de febrero de 2025
Diario Oficial disponible en la web de la Imprenta Nacional de Colombia el 21 de febrero de 2025
MINISTERIO DE SALUD Y PROTECCIÓN SOCIAL
<NOTA DE VIGENCIA: Circular derogada por la Circular 12 de 2025>
| Para: | Gobernador, Alcaldes, Secretaría Departamental y Municipales de Salud, Direcciones Locales de Salud, Entidades Promotoras de Salud, Entidades Adaptadas, Entidades que administran los Regímenes Especiales y de Excepción, Instituciones Prestadoras de Servicios de Salud (IPS) y Fondo Nacional de Salud de las Personas Privadas de la Libertad del Departamento de Tolima. |
| De: | Ministerio de Salud y Protección Social. |
| Asunto: | Alcance a la Circular 018 de 2024 “Directrices para la preparación, organización y respuesta ante la situación de alerta y emergencia en todo el territorio nacional por fiebre amarilla y se actualiza la Circular 018 de 2017 (…)” en atención al estado de emergencia sanitaria por brote de fiebre amarilla decretado en el departamento del Tolima y ampliación de la edad de aplicación a partir de los 9 meses de edad para la población del corredor endémico de las veredas priorizadas en los municipios de Cunday, Dolores, Prado, Purificación y Villarrica y demás veredas donde se presenten casos humanos o epizootias y las veredas colindantes, en estos municipios u otros, del departamento del Tolima y deroga la Circular 002 de 2025. |
| Fecha: | 18 de febrero de 2025. |
En el contexto de la Emergencia en Salud Pública por brote de fiebre amarilla en el departamento del Tolima, se han presentado 13 casos con 6 fallecimientos en el 2024 y desde enero de 2025 a la fecha, ya se han confirmado 16 casos con 6 fallecimientos para un total de 29 casos y 12 fallecimientos, alcanzando una letalidad del 41,3%. El rango de edad de los casos confirmados es de 11 a 89 años en el periodo comprendido entre el 8 de septiembre de 2024 al 8 de febrero de 2025 (fecha del último caso confirmado).
Por la situación de emergencia sanitaria este Ministerio expidió la Circular 002 de 2025 dando alcance a la Circular 018 de 2024, como medida transitoria de vacunación a población de 9 a 11 meses y 29 días, y de 60 a 69 años de edad del corredor endémico, correspondiente a 54 veredas priorizadas en los municipios de Cunday, Dolores, Prado, Purificación y Villarrica.
Según la Organización Mundial de la Salud (OMS), en su “Documento de posición sobre Vacunas y vacunación contra la fiebre amarilla de junio de 2013”, recomienda considerar la vacunación en mayores de 60 años mediante una evaluación individualizada de riesgo-beneficio(1). Además, se cuenta con experiencias internacionales, donde se ha empleado la vacuna en mayores de 60 años durante situaciones de brote(2), (3), (4), (5). Cabe destacar que el análisis beneficio-riesgo individual, debe realizarse con una perspectiva particular en la zona donde el escenario epidemiológico refuerza un alto riesgo de contraer la enfermedad, como es el caso del corredor endémico para el virus en el departamento del Tolima, donde la población ha estado expuesta naturalmente por un período prolongado.
Ante este escenario epidemiológico del departamento del Tolima, con un incremento de casos de fiebre amarilla y letalidad en población no vacunada mayor de 70 años, se considera necesario ampliar la edad de vacunación con este biológico a toda la población expuesta al brote en el corredor endémico, siendo esta una medida vital ante la no existencia de cura ni tratamiento específico para esta enfermedad de alta mortalidad que está afectando a la población susceptible independientemente de la edad.
Por lo anterior, se indica la vacunación de la población susceptible (no vacunada) a partir de los 9 meses de edad en adelante a toda la población que resida, transite o que se vaya a desplazar por las veredas priorizadas del corredor endémico para fiebre amarilla del departamento del Tolima, previa anamnesis de las condiciones de salud para detectar afecciones asociadas con inmunocompetencia alterada.
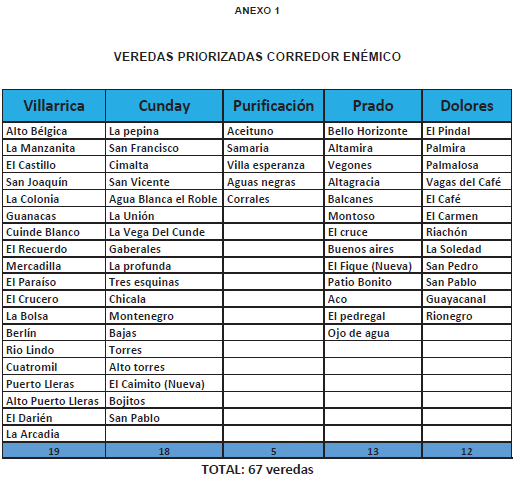
A la fecha, el corredor endémico está conformado por 67 veredas (situación dinámica) de los municipios de Cunday, Dolores, Prado, Purificación y Villarrica y se ampliará a las veredas donde se presenten casos o epizootias y a las veredas colindantes, en estos municipios u otros.
Para el resto de la población que no hace parte del corredor endémico, se le garantizará la dosis única de la vacuna contra la fiebre amarilla en los rangos de edad de 1 a 59 años, en área urbana y rural de todos los municipios del departamento del Tolima, como medida complementaria a la situación de brote.
Acorde con lo expuesto, el Ministerio de Salud y Protección Social (MSPS) en ejercicio de sus funciones, como órgano rector del Sector Salud, encargado de la dirección, orientación y conducción del Sistema de Salud de acuerdo con lo establecido en el Decreto Ley 4107 de 2011, considera necesario, derogar la Circular 002 de 2025 y emitir la presente circular externa, e impartir las siguientes directrices a los destinatarios, con medidas complementarias y transitorias a la Circular 018 de 2024.
Por lo anterior, es importante tener en cuenta los siguientes aspectos:
1. MUNICIPIOS DE ALTO RIESGO PARA FIEBRE AMARILLA (FA).
De acuerdo con la Circular 018 de 2024 mediante la cual se actualizan los municipios de alto riesgo para FA y se establece incluir como municipio de alto riesgo aquel con condiciones ecoepidemiológicas para FA, que confirme caso humano o epizootia en su investigación epidemiológica y sus municipios vecinos que cumplan con dichas condiciones; se hace necesario actualizar la lista de los municipios de alto riesgo en el departamento del Tolima, considerando la presencia de casos, así:
- Tolima: Los municipios de Alpujarra, Carmen de Apicalá, Coyaima, Cunday, Dolores, Guamo, Icononzo, Melgar, Natagaima, Prado, Purificación, Saldaña, Suárez y Villarrica.
2. ALCANCE AL PLAN DE CONTINGENCIA EN EL DEPARTAMENTO DEL TOLIMA
Frente a la evolución epidemiológica del brote y las condiciones de riesgo de la población identificada en las visitas documentadas en las veredas priorizadas de alto riesgo; en su mayoría, de alta ruralidad, se establece ampliar la edad de vacunación contra la fiebre amarilla a partir de los 9 meses de edad a la población susceptible que resida, transite o que se vaya a desplazar por el corredor endémico para el virus conformado por 67 veredas priorizadas de los municipios de Cunday, Dolores, Prado, Purificación y Villarrica (condición dinámica), ampliándose a las veredas donde se presenten casos humanos o epizootias, así como, a las veredas colindantes de estos municipios u otros. Esta medida es transitoria por parte del Ministerio de Salud y Protección Social hasta que sea superada la Emergencia Sanitaria en el departamento de acuerdo con las instrucciones dada en la Circular 018 de 2024.
Para el resto de la población que no hace parte del corredor endémico, se le garantizará la dosis única de la vacuna contra la fiebre amarilla en los rangos de edad de 1 a 59 años, en área urbana y rural de todos los municipios del departamento del Tolima.
En este sentido, teniendo en cuenta las competencias legales que, en materia de salud pública, aseguramiento y prestación de servicios le han sido asignadas a los departamentos, municipios, y demás actores a quienes va dirigida esta circular, se reiteran las obligaciones establecidas en la Ley 715 de 2001, el Decreto número 780 de 2016 Único Reglamentario del Sector Salud y Protección Social, la Resolución número 1536 de 2015 y la Resolución número 3280 de 2018, con el fin de que sean aplicables a la ejecución del Plan de Contingencia.
En concordancia con lo anterior, se establecen los siguientes ajustes en las líneas estratégicas, para ser adoptados e implementados por los destinatarios de esta circular.
2.1. LÍNEA ESTRATÉGICA DE GESTIÓN INTEGRAL DE LA CONTINGENCIA
2.1.1. A la Gobernación, Alcaldías, Secretaría de Salud Departamental, Municipales y Direcciones Locales de Salud.
(…)
2.1.1.7 Quedará así:
Elaborar e implementar el plan de acción territorializado, por parte de la Entidad Territorial - ET departamental y municipales de salud en articulación con el Programa Ampliado de Inmunizaciones PAI y en conjunto con Entidades Administradora de Planes de Beneficios EAPB, Instituciones de Prestadores de Servicios IPS y demás actores responsables y aliados estratégicos en el marco del brote de FA para la vacunación a partir de los 9 meses de edad a la población susceptible que resida, transite o que se vaya a desplazar por el corredor conformado por 67 veredas priorizadas (situación dinámica) de los municipios de Cunday, Dolores, Prado, Purificación y Villarrica. El corredor endémico se ampliará a las veredas donde se presenten casos humanos o epizootias, así como, a las veredas colindantes en estos municipios u otros.
(…)
2.1.1.25 Quedará así:
Coordinar el ingreso de la autoridad sanitaria a las zonas de difícil acceso con líderes comunitarios, incluyendo la participación de las poblaciones étnicas de la zona y aliados para la realización de intervenciones en salud pública, como la vacunación, entre otras, teniendo en cuenta las directrices relacionadas con la Misión Médica establecidas en la Resolución 4481 de 2012.
(…)
2.1.1.28 Vigilar que las EAPB e IPS garanticen la vacunación sin barreras de la población susceptible que resida o transite por el corredor endémico y demás municipios del departamento, así como, la población viajera que ingresa a ellos, de acuerdo con las indicaciones dadas en la presente circular, dando cumplimiento a la Ley 2406 de 2024.
2.1.1.29. Vigilar que se realice la notificación inmediata al SIVIGILA de cualquier caso probable o confirmado de FA incluyendo las muertes, así como, los casos sospechosos de Eventos Adversos Posteriores a la vacunación contra la fiebre amarilla (EAPV), incluyendo caso sospechoso de muerte por EAPV dando cumplimiento a todas las instrucciones dadas en los protocolos de Vigilancia para FA del INS y de Eventos Adversos Posteriores a la Vacunación - EAPV del INVIMA.
2.1.1.30 Realizar las unidades de análisis y validación para la evaluación de Eventos Adversos Posteriores a la Vacunación de fiebre amarilla de los casos notificados al Sistema de VIGIFLOW por parte del Comité Territorial de EAPV del programa permanente de acuerdo con los lineamientos del INVIMA.
2.1.2. A las Entidades Promotoras de Salud, Entidades Adaptadas, Entidades que Administran Planes Voluntarios de Salud, Entidades que Administran los Regímenes Especial y de Excepción.
(…)
2.1.2.2. Quedará así:
Evaluar la capacidad instalada o contratada con su red de prestadores de servicios de salud en el territorio y logística para garantizar la vacunación contra la fiebre amarilla a la población susceptible: 1) De 9 meses en adelante que resida, transite o que se vaya a desplazar por el corredor endémico conformado por 67 veredas priorizadas de los municipios de Cunday, Dolores, Prado, Purificación y Villarrica (situación dinámica). El corredor endémico se ampliará a las veredas donde se presenten casos humanos o epizootias, así como, a las veredas colindantes en estos municipios u otros; 2) De 1 a 59 años en el resto de veredas y municipios del departamento para la población que no haga parte del corredor endémico.
2.1.2.3. Quedará así:
Realizar de manera articulada con la Secretaría de Salud y su red prestadora de servicios de salud, la microplanificación del territorio, para establecer las estrategias y tácticas necesarias que aseguren coberturas de vacunación del 95% de la población objetivo de esta circular.
(…)
2.1.2.5. Quedará así:
Garantizar la disponibilidad, suficiencia y completitud de la oferta de servicios de salud, capacidad instalada y tecnologías en salud para el diagnóstico y la atención de los casos de FA, eliminando las barreras geográficas para el acceso a los servicios de salud, entregando al departamento la ruta de atención.
2.1.2.6. Quedará así:
Organizar y gestionar la red de prestadores de servicios de salud para la atención integral de los Eventos Adversos Posteriores a la Vacunación (EAPV), la confirmación diagnóstica y el seguimiento, entregando al departamento la ruta de atención.
2.1.2.7. Quedará así:
Hacer seguimiento y monitoreo a la oportunidad en la atención integral de casos de FA y Eventos Adversos Posteriores a la Vacunación (EAPV), para lo cual se deberá verificar tiempos y reducirlos cuando sea pertinente a través de acuerdos con las IPS contratadas.
2.1.2.8. Quedará así:
Ajustar de manera expedita los trámites administrativos para eliminar el proceso de autorizaciones de la población con sospecha o diagnóstico de FA, así como, de Eventos Adversos Posteriores a la Vacunación (EAPV) de acuerdo con lo establecido en el artículo 2.5.3.4.7.4. del Decreto número 780 de 2016 Único Reglamentario del sector Salud y Protección Social.
(…)
2.1.2.10. Garantizar la contratación de la red prestadora de servicios de salud, de tal forma que cubra las necesidades de los usuarios frente a la vacunación, dando cumplimiento a las estrategias de vacunación sin barreras establecidas en la Ley 2406 de 2024.
2.1.3. A las Instituciones Prestadoras de Servicios de Salud (IPS)
(…)
2.1.3.5. Las Instituciones de Servicios de Salud de la red pública y privada con servicios de urgencias activos deberán reportar con carácter obligatorio y a diario las capacidades hospitalarias para emergencias en el siguiente link:
https://ee.humanitarianresponse.info/x/KMLBnHKT
Y sus afectaciones en el siguiente link:
https://forms.office.com/r/RfUrhafdwb?origin=IprLink
El reporte se hará a las 18:00 horas.
2.1.3.6. Las Instituciones de Servicios de Salud deben mantener el medio de comunicación con el Centro Regulador de Urgencias, Emergencias y Desastres de su jurisdicción y facilitar la operación del sistema de referencia y contrarreferencia; informar sobre los casos con indicación de remisión para realizar de forma oportuna el traslado de pacientes en la red de prestadores definida por la Entidad Promotora de Salud en el marco de las redes de la EPS a través del proceso de referencia y contrarreferencia para garantizar la oportunidad y continuidad de la atención de los pacientes.
Las demás acciones e indicadores de la línea estratégica de gestión integral de la contingencia se mantienen incólumes de acuerdo con la Circular 018 de 2024.
2.2. LÍNEA ESTRATÉGICA DE INTENSIFICACIÓN DE LA VIGILANCIA EN SALUD PÚBLICA
2.2.1. A la Secretaría de Salud Departamental, Municipales, Direcciones Locales de Salud o la entidad que haga sus veces
(…)
2.2.1.2. Quedará así:
Fortalecer la red de vigilancia epidemiológica de la red de prestación de servicios de salud, mediante asistencia técnica, difusión, socialización y seguimiento al cumplimiento del protocolo de vigilancia de FA disponible en https://www.ins.gov.co/buscador-eventos/ Lineamientos/310_F_Amarilla_2024.pdf y https://www.ins.gov.co/buscador-eventos/ Lineamientos/Pro_Fiebre%20amarilla%202024.pdf, así como, del lineamiento de Eventos Adversos Posteriores a la Vacunación - EAPV del INVIMA, disponible en:
https://www.invima.gov.co/sites/default/files/medicamentos-productos-biologicos/ Medicamentos%20de%20s%C3%ADntesis%20qu%C3%ADmica%20y%20 biol%C3%B3gica/Vigilancia/Programa-Nacioal-de-Farmacovigilancia/Formatos-tramites-y-guias/2024/Lineamientos%20vacunacio%CC%81n%20EAPV.pdf garantizando el funcionamiento del sistema de vigilancia y la calidad de la información según las responsabilidades establecidas.
2.2.1.3. Quedará así:
Asegurar la notificación inmediata a SIVIGILA de cualquier caso probable o confirmado de FA incluyendo las muertes, así como, casos graves sospechosos de Eventos Adversos Posteriores a la Vacunación por fiebre amarilla (EAPV), incluyendo caso sospechoso de muerte por EAPV y realizar en las primeras 48 horas la investigación epidemiológica de campo, contemplando la búsqueda comunitaria e institucional, según lo estipulado en el protocolo de vigilancia en salud pública. Comunicar de manera inmediata al Centro Nacional de Enlace al correo cne@minsalud.gov.co y al Equipo de Respuesta Inmediata (ERI), Instituto Nacional de Salud - INS al correo eri@ins.gov.co dando cumplimiento a todas las instrucciones dadas en los respectivos protocolos y lineamientos nacionales del INS y del INVIMA.
(…)
2.2.1.12. Articular la respuesta y el seguimiento de Eventos Adversos Posteriores a la Vacunación (EAPV) contra la fiebre amarilla por parte del INS- INVIMA de acuerdo con los protocolos y lineamientos existentes.
2.2.1.13. Realizar las acciones de Monitoreo Rápido de Vacunación (MRV) por parte de Vigilancia epidemiológica en áreas donde se sospecha el contagio de FA, en la población de 9 meses de edad en adelante en las 67 veredas priorizadas del corredor endémico de los municipios de Cunday, Dolores, Prado, Purificación y Villarrica (Condición dinámica). El corredor endémico se ampliará a las veredas donde se presenten casos humanos o epizootias, así como, a las veredas colindantes, en estos municipios u otros.
2.2.1.14. Apoyar la conformación de la red territorial de vigilancia basada en la comunidad para identificar de manera oportuna los casos probables de FA o posibles focos de transmisión, así como, los casos sospechosos de EAPV por fiebre amarilla.
2.2.1.15. Informar de manera inmediata los Eventos Adversos Posteriores a la Vacunación (EAPV) contra la fiebre amarilla al referente de farmacovigilancia (FV) de la entidad territorial para este articularse con el INS, el INVIMA y el PAI Nacional y Vigilar que sea notificado en el Sistema de VIGIFLOW del INVIMA los casos sospechosos de EAPV por fiebre amarilla, así como, los casos confirmados por cepa vacunal garantizando los trámites pertinentes.
2.2.1.16. Realizar las unidades de análisis y validación de los casos de Eventos Adversos Posteriores a la Vacunación (EAPV) por fiebre amarilla por parte del Comité Territorial de EAPV del programa permanente y remitir de manera oportuna de acuerdo a los lineamientos nacionales del INVIMA.
(…)
2.2.4. A las Entidades Promotoras de Salud, Entidades Adaptadas, Entidades que Administran Planes Voluntarios de salud, Entidades que Administran lo Regímenes Especial y de Excepción y el Fondo Nacional de Salud de las Personas Privadas de la Libertad.
2.2.4.1. Quedará así:
Realizar análisis de la situación epidemiológica del evento en sus afiliados, de estos análisis se formularán los planes de acción para tomar medidas oportunas frente a la alerta por casos de FA o de Eventos Adversos Posteriores a la Vacunación (EAPV) contra la FA.
(…)
2.2.4.3. Quedará así:
Garantizar la contratación con la red prestadora de servicios de salud, para la realización de necropsia clínica ante muerte de un caso probable de FA o muerte por Evento Adverso Posterior a la Vacunación - EAPV contra la FA.
2.2.5. A las instituciones Prestadoras de Servicios de Salud Públicas y Privadas
2.2.5.1. Quedará así:
Realizar la notificación inmediata a SIVIGILA de cualquier caso probable o confirmado de FA incluyendo las muertes, así como, los casos graves sospechosos de Eventos Adversos Posteriores a la Vacunación contra la fiebre amarilla - EAPV, incluyendo caso sospechoso de muerte por EAPV dando cumplimiento a todas las instrucciones dadas en los respectivos protocolos y lineamientos nacionales del INS y del INVIMA garantizando el funcionamiento del sistema de vigilancia y la calidad de la información según las responsabilidades establecidas en:
Protocolo de atención de caso y los lineamientos en Salud Pública de vigilancia de FA disponible en https://www.ins.gov.co/buscador-eventos/Lineamientos/310_F_ Amarilla_2024.pdf y https://www.ins.gov.co/buscador-eventos/Lineamientos/Pro_ Fiebre%20amarilla%202024.pdf.
Lineamiento de Eventos Adversos Posteriores a la Vacunación (EAPV) del INVIMA, disponible en:
https://www.invima.gov.co/sites/default/files/medicamentos-productos-biologicos/ Medicamentos%20de%20s%C3%ADntesis%20qu%C3%ADmica%20y%20 biol%C3%B3gica/Vigilancia/Programa-Nacioal-de-Farmacovigilancia/Formatos-tramites-y-guias/2024/Lineamientos%20vacunacio%CC%81n%20EAPV.pdf.
(…)
2.2.5.3. Realizar la notificación de los casos de Eventos Adversos Posteriores a la Vacunación (EAPV) contra la fiebre amarilla sospechosos o confirmados por cepa vacunal al Sistema de VIGIFLOW, según lo establecido en los lineamientos nacionales del INVIMA.
2.2.5.4. Participar en las unidades de análisis y validación de los casos de Eventos Adversos Posteriores a la Vacunación (EAPV) por fiebre amarilla por parte del Comité Territorial de EAPV del programa permanente según lo establecido en los lineamientos nacionales del INVIMA.
2.2.6. A los Centros Reguladores de Urgencias, Emergencias y Desastres (CRUE)
2.2.6.1. Remitir a la instancia de vigilancia en salud pública territorial en caso de recibir información de cualquier fuente sobre casos probables o confirmados de FA, incluido rumor de epizootias o de Eventos Adversos por Vacunación de fiebre amarilla (EAPV) con el fin de que se realicen las acciones pertinentes.
2.2.6.2. Mantener un canal de información permanente con el Consejo Departamental de Gestión del Riesgo con el fin de articular y coordinar las acciones y apoyos necesarios con los demás sectores que sea necesarios para cumplir con las acciones de vacunación.
2.2.7. Indicadores
Tabla 2. Se adicionan los siguientes Indicadores de seguimiento a las acciones de la línea de intensificación de la vigilancia en salud pública.
| Indicador | Definición operacional | Entidad responsable | Periodicidad |
| Cumplimiento y cargue al Vigiflow de las unidades de análisis de Eventos Adversos Posterior a la Vacunación - EAPV contra la FA. | Número de EAPV validados en unidades de análisis y cargados en Vigiflow/ Número de EAPV notificados al Sistema de Vigiflow, según los tiempos establecidos en los lineamientos nacionales de Invima de EAPV. | Secretaría de Salud Departamental del Tolima | Semanal |
| Porcentaje de Eventos Adversos Leves Posterior a la vacunación – EAPV contra la FA en población de 60 y más años. | N° de EAPV leves contra la FA en población de 60 y más años / población vacunada de 60 y más años en el corredor endémico *100. | Secretaría de Salud Departamental del Tolima | Semanal |
| Porcentaje de Eventos Adversos Graves Posterior a la vacunación – EAPV contra la FA en población de 60 y más años. | N° de EAPV graves contra la FA en población de 60 y más años / población vacunada de 60 y más años en el corredor endémico *100. | Secretaría de Salud Departamental del Tolima | Semanal |
| Porcentaje de Eventos Adversos Leves Posterior a la vacunación – EAPV contra la FA en población de 9 a 11 meses y 29 días. | N° de EAPV leves contra la FA en población de 9 a 11 meses y 29 días / población vacunada de 9 a 11 meses y 29 días en el corredor endémico *100. | Secretaría de Salud Departamental del Tolima | Semanal |
| Porcentaje de Eventos Adversos Graves Posterior a la vacunación – EAPV contra la FA en población de 9 a 11 meses y 29 días. | N° de EAPV graves contra la FA en población de 9 a 11 meses y 29 días / población vacunada de 9 a 11 meses y 29 días en el corredor endémico *100. | Secretaría de Salud Departamental del Tolima | Semanal |
| Porcentaje de Eventos Adversos Graves Posterior a la vacunación – EAPV contra la FA en población de 1 a 59 años. | N° de EAPV graves contra la FA en población de 1 a 59 años/ población vacunada de 1 a 59 años en el departamento *100. | Secretaría de Salud Departamental del Tolima | Semanal |
| Porcentaje de EAPV notificados por Vigiflow por parte de la ET | Número de EAPV notificados en Vigiflow/ Número de EAPV identificados según los lineamientos nacionales de Invima de EAPV. | IPS | Semanal |
Las demás acciones e indicadores de la Línea Estratégica de Intensificación de la Vigilancia en Salud Pública se mantienen incólumes de acuerdo con la Circular 018 de 2024.
2.3. LÍNEA ESTRATÉGICA DE PROMOCIÓN DE LA SALUD Y PREVENCIÓN PRIMARIA DE LA TRANSMISIÓN
2.3.1. Vacunación para la prevención de la transmisión y reducción de morbilidad
2.3.1.1. A la gobernación, alcaldías, secretarías de salud (departamental y municipales), Direcciones Locales de Salud o la entidad que haga sus veces
2.3.1.1.1. Quedará así:
Realizar con las EAPB y su red prestadora de servicios de salud la microplanificación del territorio para el fortalecimiento de las coberturas de vacunación con la dosis única de por vida contra la FA de la población susceptible, incluyendo la georreferenciación y programación en áreas priorizadas, estableciendo las estrategias y tácticas necesarias que garanticen la vacunación contra la fiebre amarilla de la población susceptible 9 meses de edad y más que resida, transite o que se vaya a desplazar por el corredor endémico conformado por las 67 veredas priorizadas de los municipios de Cunday, Dolores, Prado, Purificación y Villarrica (situación dinámica), ampliándose a las veredas donde se presenten casos humanos o epizootias, así como, a las veredas colindantes en estos municipios u otros.
2.3.1.1.2. Quedará así:
Coordinar las acciones de Monitoreo Rápido de Vacunación (MRV) por parte de Vigilancia y la Vacunación por Barrido Documentado por parte del PAI de la población a partir de 9 meses de edad del corredor endémico, garantizando TH para lograr coberturas superiores al 95%, tanto en área urbana como rural, dando cumplimiento a los requisitos exigidos previos y posterior a la vacunación contra la FA. El corredor endémico se ampliará a las veredas donde se presenten casos humanos o epizootias, así como, a las veredas colindantes en estos municipios u otros.
(…)
2.3.1.1.4. Quedará así:
Verificar la notificación oportuna de dosis aplicadas contra la FA de 9 a 11 meses y 29 días, 1 a 59 años y de 60 y más años, en área urbana y rural, por parte de los prestadores de servicios de salud, diario o semanal según la evolución del brote.
2.3.1.1.5. Quedará así:
Realizar capacitación al grupo ERI frente al brote y frente a la ampliación de la vacunación contra la FA en esta región.
2.3.1.1.6. Quedará así:
Capacitación y/o reinducción en los componentes del PAI, vacunación segura, vacuna contra la fiebre amarilla y eventos adversos posteriores a la vacunación, al talento humano en salud de las IPS y Equipos Básicos de Salud, haciendo énfasis en la población objeto a vacunar establecido en la presente circular.
(…)
2.3.1.1.8. Quedará así:
Realizar seguimiento al cumplimiento del registro obligatorio y oportuno de dosis aplicadas, así como el registro de observaciones pertinentes, por parte de los prestadores, en el sistema de información nominal de vacunación PAIWEB, así mismo, verificar la calidad del dato de las dosis registradas.
2.3.1.1.9. Quedará así:
Coordinar que las EAPB de régimen de excepción (Fuerzas Militares (FF. MM.), Policía Nacional (PONAL), entre otros) y Fondo Nacional de Salud de las PPL (Personas Privadas de la Libertad), realicen la búsqueda y vacunación de su población susceptible a partir de los 9 meses de edad del corredor endémico.
2.3.1.1.10. Verificar que las EAPB garanticen a través de su red de prestación de servicios, el talento humano profesional en medicina y enfermería capacitado para realizar la anamnesis y el diligenciamiento de los diferentes formatos previos a la vacunación de la población de 60 y más años que resida, transite o que se vaya a desplazar por el corredor endémico del departamento del Tolima, con el fin de identificar antecedentes y condiciones de salud que pudiesen contraindicar la vacunación, propendiendo por el control de reacciones anafilácticas y eventuales eventos adversos posteriores a la vacunación.
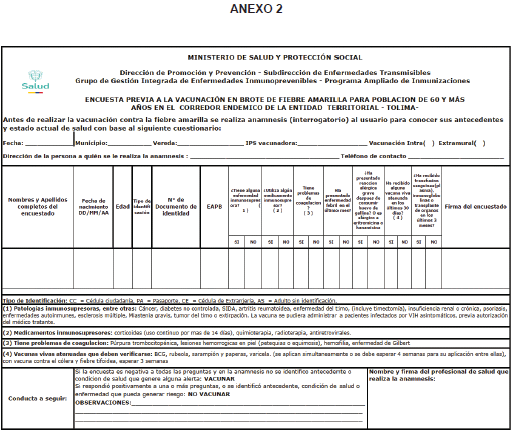
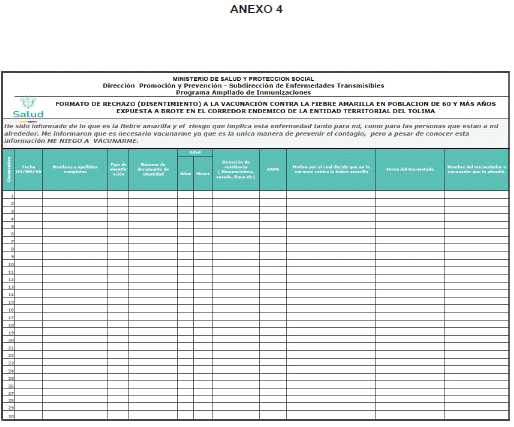
2.3.1.1.11. Difundir los formatos anexos a la presente circular, cuyo diligenciamiento debe estar a cargo de los profesionales de la salud de las IPS (médico, enfermera), incluido los Equipos Básicos de Salud (médico, enfermera), siendo un requisito previo a la vacunación, los cuales son: “Consentimiento informado para la aplicación de la vacuna contra la fiebre amarilla en población de 60 y más años en el corredor endémico por brote de FA del Tolima”, “Encuesta previa a la vacunación en brote de fiebre amarilla para la población de 60 y más años del corredor endémico del Tolima” y “Formato de rechazo a la vacunación contra la fiebre amarilla en población de 60 y más años expuesta a brote en la ET Tolima”, con el fin de detectar y declarar condiciones de salud que pudiesen ser contraindicación para la vacuna.
2.3.1.1.12. Los anexos que hacen parte integral de esta circular serán suministrados por parte de este Ministerio a la ET departamental, quien será responsable de su socialización y capacitación y su uso es exclusivo para el departamento del Tolima.
2.3.1.1.13. Verificar que las EAPB garanticen a través del TH en salud de las IPS, el seguimiento y registro de las condiciones de salud de la población vacunada de 60 y más años entre 5 a 7 días, entre 15 a 18 días y a los 30 días para identificar signos y síntomas sospechosos de EAPV - Eventos Adversos Posteriores a la Vacunación y generen la atención domiciliaria y/o hospitalaria pertinente y oportuna, así como, las respectivas notificaciones inmediatas en SIVIGILA, VIGIFLOW y comunicación a la ET.
2.3.1.1.14. Verificar que las EAPB – IPS dejen constancia de cada seguimiento posvacunación; presencial, virtual, llamada telefónica, jornadas de salud, entre otras estrategias que se apliquen en esta área rural y rural dispersa del corredor endémico, incluso, seguimiento articulado con las juntas de acción comunal o demás asociaciones de aquellas zonas rurales de difícil acceso.
2.3.1.1.15. Constatar para la vacunación de la población de 9 a 11 meses y 29 días que resida, transite o que se vaya a desplazar por el corredor endémico, que realice el interrogatorio habitual que se practica por parte de los vacunadores para conocer el estado de salud y detectar antecedentes y condiciones de riesgo que pudiesen contraindicar la vacunación. Esta dosis corresponde a la dosis del esquema, no requiere refuerzo ni a los 12 ni a los 18 meses.
2.3.1.1.16. Consolidar 1) Informe de vacunación y seguimiento al Plan de Acción territorializado e indicadores. 2) Informe de EAPV leves y graves y reporte de indicadores con periodicidad mensual.
2.3.1.1.17. Conformar bajo acto administrativo y/o activar el comité de expertos territorial para la evaluación de eventos adversos graves por vacunación contra la fiebre amarilla y la realización de unidades de análisis para la clasificación de los casos.
2.3.1.2. A las Entidades Promotoras de Salud, Entidades Adaptadas, Entidades que Administran Planes Voluntarios de Salud, Entidades que Administran los Regímenes Especial y de Excepción
2.3.1.2.1. Quedará así:
Evaluar la capacidad instalada o contratada con su red de prestadores de servicios de salud en el territorio y la logística para garantizar la vacunación contra la FA por barrido documentado de toda la población susceptible a partir de los 9 meses de edad que resida, transite o que se vaya a desplazar por el corredor endémico para el virus de fiebre amarilla conformado por 67 veredas priorizadas de los municipios de Cunday, Dolores, Prado, Purificación y Villarrica (situación dinámica), ampliándose a las veredas donde se presenten casos humanos o epizootias y a las veredas colindantes en estos municipios u otros; así como, la vacunación sin barreras de la población susceptible de 1 a 59 años en el resto del departamento.
2.3.1.2.2. Quedará así:
Realizar con la ET departamental y municipales del Tolima y la red prestadora de servicios de salud, la microplanificación del corredor endémico del territorio para garantizar a través de barrido documentado y demás estrategias (extramural e intramural) y tácticas de impacto para asegurar coberturas de vacunación contra la FA del 95% (urbano y rural) en la población de 9 meses y más años del corredor endémico.
2.3.1.2.3. Quedará así:
Garantizar el reporte diario y semanal de dosis aplicadas contra la FA de la población vacunada de 9 a 11 meses y 29 días, 1 a 59 años y de 60 y más en área urbana y rural por parte de los prestadores de servicios de salud.
(…)
2.3.1.2.5. Quedará así:
Realizar seguimiento al avance de la población vacunada contra la FA en el marco y en cumplimiento del Plan de Acción Territorializado y verificar el registro oportuno de dosis y observaciones pertinentes en el sistema de información nominal de vacunación PAIWEB por parte de sus prestadores.
2.3.1.2.6. Quedará así:
Asegurar la atención en salud, notificación en VIGIFLOW y seguimiento a Eventos Adversos Posteriores a la Vacunación - EAPV contra la FA por parte de sus prestadores.
2.3.1.2.7. Garantizar a través de su red de prestación de servicios, el talento humano profesional en medicina y enfermería capacitados para realizar la anamnesis y el diligenciamiento de los diferentes formatos previos a la vacunación de la población de 60 y más años que resida, transite o que se vaya a desplazar por el corredor endémico del departamento del Tolima, con el fin de identificar antecedentes y condiciones de salud que pudiesen contraindicar la vacunación, propendiendo por el control de reacciones anafilácticas y eventuales eventos adversos posteriores a la vacunación.
2.3.1.2.8. Garantizar a través de las IPS la disposición de copias físicas para el diligenciamiento de los formatos anexos a la presente circular, por parte de los profesionales de la salud de las IPS (médico, enfermera), requisito obligatorio previo a la vacunación de la población de 60 y más años, los cuales son: “Consentimiento informado para la aplicación de la vacuna contra la fiebre amarilla en población de 60 y más años en el corredor endémico por brote de FA del Tolima”, “Encuesta previa a la vacunación en brote de fiebre amarilla para la población de 60 y más años del corredor endémico del Tolima” y “Formato de rechazo a la vacunación contra la fiebre amarilla en población de 60 y más años expuesta a brote en la ET Tolima”. La socialización y capacitación de los mencionados formatos estará a cargo de las ET y son de uso exclusivo para el departamento del Tolima.
2.3.1.2.9. Garantizar a través de su red de prestación de servicios el TH en salud que realice el seguimiento y registro de las condiciones de salud de la población vacunada de 60 y más años entre 5 a 7 días, entre 15 a 18 días y a los 30 días posteriores a la vacunación, para identificar signos y síntomas sospechosos de EAPV - Eventos Adversos Posteriores a la Vacunación y generar la atención domiciliaria y/o hospitalaria pertinente y oportuna, así como, las respectivas notificaciones inmediatas en SIVIGILA, VigiFlow y comunicación a la ET. Verificar que quede constancia de cada seguimiento posvacunación; presencial, virtual, llamada telefónica, jornadas de salud, entre otras estrategias que apliquen en esta área rural dispersa del corredor endémico, incluso, articular seguimiento de estas personas vacunadas con las juntas de acción comunal o demás asociaciones de aquellas zonas de difícil acceso.
2.3.1.2.10. Verificar y registrar semanalmente los soportes de seguimiento de las personas vacunadas de 60 y más años para dar constancia de su estado de salud.
2.3.1.3. A las Instituciones Prestadoras de Servicios de Salud (IPS)
2.3.1.3.1. Quedará así:
Realizar capacitación y/o reinducción en los componentes del PAI, vacunación segura, vacuna contra la fiebre amarilla y eventos adversos posteriores a la vacunación al talento humano en Salud de las IPS y de los Equipos Básicos de Salud, haciendo énfasis en la ampliación de la población objeto a vacunar.
(…)
2.3.1.3.4. Quedará así:
Mediante la microplanificación establecer las estrategias de vacunación intramural y extramural contra la FA, así como, las tácticas necesarias (barrido documentado, concentración, casa a casa, ampliación de horarios, entre otras) de acuerdo con las características del territorio para la búsqueda y vacunación de la población susceptible de 9 meses y más años que resida, transite o que se vaya a desplazar por el corredor endémico para el virus de fiebre amarilla conformado por 67 veredas priorizadas de los municipios de Cunday, Dolores, Prado, Purificación y Villarrica (situación dinámica) ampliándose a las veredas donde se presenten casos humanos o epizootias, así como, a las veredas colindantes en estos municipios u otros. Lo anterior, para asegurar coberturas de vacunación del 95% y más en el corredor endémico (área urbana y rural) para alcanzar el Control de la Emergencia Sanitaria por FA.
2.3.1.3.5. Quedará así:
Disponer del talento humano en salud suficiente y capacitado, así como la logística, para poder garantizar la vacunación contra la FA mediante barrido documentado de la población susceptible de 9 meses y más años del corredor endémico; así como, la vacunación de la población susceptible de 1 a 59 años en el resto del departamento, mediante estrategias intra y extramural y tácticas de impacto en articulación con las ET y EAPB del territorio.
Las IPS deben garantizar el talento humano profesional en medicina y enfermería incluido los equipos básicos de salud (médico, enfermera) así como el personal disponible en cada territorio, capacitado para realizar la anamnesis y el diligenciamiento de los diferentes formatos previos a la vacunación de la población de 60 y más años que resida, transite o que se vaya a desplazar por el corredor endémico, con el fin de identificar antecedentes y condiciones de salud que pudiesen contraindicar la vacunación, propendiendo por el control de reacciones anafilácticas y eventuales eventos adversos posteriores a la vacunación.
(…)
2.3.1.3.7. Quedará así:
Realizar la respectiva notificación y atención de los Eventos Adversos Posteriores a la Vacunación (EAPV) por FA de acuerdo con los protocolos del INS y lineamientos del INVIMA garantizando el funcionamiento del sistema de vigilancia y la calidad de la información según las responsabilidades establecidas.
Protocolo de Vigilancia de FA del INS, disponible en https://www.ins.gov.co/buscador-eventos/Lineamientos/310_F_Amarilla_2024.pdf y https://www.ins.gov.co/buscador-eventos/Lineamientos/Pro_Fiebre%20amarilla%202024.pdf.
Lineamiento de Eventos Adversos Posteriores a la Vacunación (EAPV) del INVIMA, disponible en:
https://www.invima.gov.co/sites/default/files/medicamentos-productos-biologicos/ Medicamentos%20de%20s%C3%ADntesis%20qu%C3%ADmica%20y%20 biol%C3%B3gica/Vigilancia/Programa-Nacioal-de-Farmacovigilancia/Formatos-tramites-y-guias/2024/Lineamientos%20vacunacio%CC%81n%20EAPV.pdf.
(…)
2.3.1.3.9. Quedará así:
Reportar diariamente a las ET correspondientes, las dosis aplicadas de vacuna contra la FA, en área urbana y rural de 9 a 11 meses y 29 días, de 1 a 59 años y de 60 y más años.
2.3.1.3.10. Quedará así:
Registrar de manera obligatoria y oportuna las dosis aplicadas contra la FA y las observaciones pertinentes en el sistema de información nominal nacional PAIWEB, dando cumplimiento a la calidad del dato de estos registros.
(…)
2.3.1.3.12. Quedará así:
Para la vacunación de la población de 9 a 11 meses y 29 días que resida, transite o que se vaya a desplazar por el corredor endémico, se realizará el interrogatorio habitual que se practica por parte de los vacunadores para conocer el estado de salud y detectar antecedentes y condiciones de riesgo que pudiesen contraindicar la vacunación. Esta dosis corresponde a la dosis del esquema, no requiere refuerzo ni a los 12 ni a los 18 meses.
(…)
2.3.1.3.16. Las IPS deberán disponer copias físicas de los formatos anexos a la presente circular para garantizar el diligenciamiento previo a la vacunación por parte de los profesionales de la salud de las IPS (médico, enfermera), incluidos los equipos básicos de salud y demás personal disponible en cada territorio, siendo un requisito obligatorio previo a la vacunación de la población de 60 y más años, los cuales son: “Consentimiento informado para la aplicación de la vacuna contra la fiebre amarilla en población de 60 y más años en el corredor endémico por brote de FA del Tolima”, “Encuesta previa a la vacunación en brote de fiebre amarilla para la población de 60 y más años del corredor endémico del Tolima” y “Formato de rechazo a la vacunación contra la fiebre amarilla en población de 60 y más años expuesta a brote en la ET Tolima”. La socialización y capacitación de los mencionados formatos estará a cargo de las ET y son de uso exclusivo para el departamento del Tolima.
2.3.1.3.17. Se debe garantizar por parte de las EAPB a través del TH en salud de las IPS, el seguimiento de las condiciones de salud de la población vacunada de 60 y más años entre 5 a 7 días, entre 15 a 18 días y a los 30 días, para identificar signos y síntomas sospechosos de Eventos Adversos Posteriores a la Vacunación (EAPV), para generar la atención domiciliaria y/u hospitalaria pertinente y oportuna, así como, la respectiva notificación inmediata en SIVIGILA como un caso probable de fiebre amarilla si corresponde a un evento grave y simultáneamente en la plataforma VigiFlow del INVIMA, además de comunicar de manera inmediata a la ET.
Se dejará constancia de cada seguimiento posvacunación. Se podrán implementar diferentes estrategias; seguimiento presencial, virtual, llamada telefónica, jornadas de salud, entre otras que apliquen en esta área rural y rural dispersa del corredor endémico. Se podrá articular el seguimiento a través de las juntas de acción comunal o demás asociaciones de aquellas zonas de difícil acceso.
2.3.1.3.18. Suministrar cada semana a la ET correspondiente y a las EAPB 1) Relación de personas vacunadas con los respectivos soportes previos a la vacunación (anexos) de la población de 60 y más años, y los soportes de seguimiento al estado de salud posvacunación de la población de 60 y más años. 2) Informe de EAPV leves y graves.
(…)
2.3.1.5. Indicadores.
Tabla 3. Se adicionan los siguientes Indicadores de seguimiento a las acciones de la línea de promoción y prevención primaria de la transmisión. Quedará así:
| Indicador | Definición operacional | Entidad responsable | Periodicidad |
| Coberturas de vacunación contra la FA en población de 60 y más años del corredor endémico. | N° de dosis aplicadas de 60 y más años en el corredor endémico / población identificada por barrido documentado de 60 y más años en el corredor endémico *100. | Secretaría de salud del nivel departamental y municipal o quien haga sus veces, aseguradoras y prestadores de servicios de salud. | Mensual |
| Porcentaje de contraindicación a la vacunación contra la FA en población de 60 y más años del corredor endémico. | N° de Encuesta previa a la vacunación en brote de fiebre amarilla con contraindicación para la vacunación de la población de 60 y más años / población identificada por barrido documentado de 60 y más años en el corredor endémico *100. | Secretaría de salud del nivel departamental y municipal o quien haga sus veces, aseguradoras y prestadores de servicios de salud. | Mensual |
| Porcentaje de Rechazo a la vacunación contra la FA en población de 60 y más años del corredor endémico. | N° de Formatos de rechazo a la vacunación contra la fiebre amarilla en población de 60 y más años/ población identificada por barrido documentado de 60 y más años en el corredor endémico *100. | Secretaría de salud del nivel departamental y municipal o quien haga sus veces, aseguradoras y prestadores de servicios de salud. | Mensual |
| Porcentaje de Consentimientos informados para la aplicación de la vacuna contra la FA en población de 60 y más años del corredor endémico. | N° de Consentimientos informados para la aplicación de la vacuna contra la fiebre amarilla en población de 60 y más años/ población identificada por barrido documentado de 60 y más años en el corredor endémico *100. | Secretaría de salud del nivel departamental y municipal o quien haga sus veces, aseguradoras y prestadores de servicios de salud. | Mensual |
| Coberturas de vacunación contra la FA en población 9 a 11 meses y 29 días del corredor endémico. | N° de dosis aplicadas en población de 9 a 11 meses y 29 días en el corredor endémico / población identificada por barrido documentado de 9 a 11 meses y 29 días en el corredor endémico *100. | Secretaría de salud del nivel departamental y municipal o quien haga sus veces, aseguradoras y prestadores de servicios de salud. | Mensual |
(…)
Las demás acciones e indicadores de la Línea de Promoción y Prevención Primaria de la Transmisión se mantienen incólumes de acuerdo con la Circular 018 de 2024.
2.4. LÍNEA ESTRATÉGICA DE ATENCIÓN INTEGRAL DE CASOS
2.4.1. A la gobernación, alcaldías, secretaría de salud departamental y municipales o entidad que haga sus veces
(…)
2.4.1.12. Quedará así:
Implementar la vigilancia centinela: capacitación sobre la captación de casos sospechosos de FA o Eventos Adversos Posterior a la Vacunación (EAPV) con el personal de laboratorio, urgencias, epidemiología y coordinaciones médicas de las IPS.
(…)
2.4.1.17. Establecer y/o activar el cumplimiento del Lineamiento de Eventos Adversos Posteriores a la Vacunación (EAPV) del INVIMA por parte de los Prestadores de Servicios de Salud, disponible en:
https://www.invima.gov.co/sites/default/files/medicamentos-productos-biologicos/ Medicamentos%20de%20s%C3%ADntesis%20qu%C3%ADmica%20y%20 biol%C3%B3gica/Vigilancia/Programa-Nacioal-de-Farmacovigilancia/Formatos-tramites-y-guias/2024/Lineamientos%20vacunacio%CC%81n%20EAPV.pdf.
2.4.1.18. Hacer seguimiento a la detección, atención en salud, notificación en VIGIFLOW y seguimiento de los casos de Eventos Adversos Posterior a la Vacunación - EAPV por fiebre amarilla, por parte de los Prestadores de Servicios de Salud.
2.4.2. A las Entidades Promotoras de Salud, Entidades Adaptadas, Entidades que Administran Planes Voluntarios de Salud, Entidades que Administran los Regímenes Especial y de Excepción
(…)
2.4.2.9. Garantizar la captación, atención en salud, notificación y seguimiento de EAPV por vacuna de fiebre amarilla por parte de los Prestadores de Servicios de Salud de su población afiliada, de acuerdo con el lineamiento de Eventos Adversos Posteriores a la Vacunación (EAPV) del INVIMA.
2.4.3. A las Instituciones Prestadoras de Servicios de Salud públicas y privadas
(…)
2.4.3.11. Garantizar la atención en salud, notificación en VIGIFLOW y seguimiento de Eventos Adversos Posterior a la Vacunación (EAPV) por vacuna de fiebre amarilla.
2.4.3.12. Desarrollar y aplicar los mecanismos para la detección, análisis y evaluación de los Eventos Adversos Posterior a la Vacunación (EAPV) por parte de las IPS que prestan el servicio de salud o las IPS vacunadoras por parte del referente de Farmacovigilancia con apoyo del referente PAI y mesas de trabajo interdisciplinarias.
Las demás acciones e indicadores de la línea Estratégica de Atención Integral de Casos, así como, la línea Estratégica de Comunicación de Riesgo y Comunicación Asertiva para la Salud y el numeral 3. Inspección Vigilancia y Control de la Superintendencia Nacional de Salud se mantienen incólumes de acuerdo con la Circular número 018 de 2024.


![]()
![]()


La presente circular deroga la Circular número 002 de 2025.
Publíquese, comuníquese y cúmplase.
Dada en Bogotá, D. C., a 18 de febrero de 2025.
EL Ministro de Salud y Protección Social,
Guillermo Alfonso Jaramillo Martínez
NOTAS AL FINAL:
1. World Health Organization. (2013). Weekly Epidemiological Record, 2013, vol. 88, 27 [full issue]. Weekly Epidemlological Record = Relevé épidémiologique hebdomadaire, 88 (27), 269-284. https:// iris.who.inVhandle/10665/242091.
2. Vargas-Leguás, H. (2010). Brote de fiebre amarilla en Paraguay en 2008: una experiencia para aprender. Enferm. emerg, 150-154.
3. Fiebre amarilla y virus del Nilo occidental - Revista de Enfermedades Infecciosas Emergentes (REIE); vol. 5-6 II Jornada Platense de Salud Pública, Enfermedades Emergentes y Zoonóticas (La Plata, 2010) Facultad de Ciencias Veterinarias ISSN: 0329-8493 Páginas: 10-12 - http://sedici.unlp.edu.ar/ handle/10915/92831.
4. Estudio comparativo de los efectos adversos tras la vacunación contra la fiebre amarilla entre viajeros de edad avanzada y no avanzada: encuesta mediante cuestionario en Japón durante un periodo de un año. https://dol.org/10. 1093/jtm/taw012.
5. Evaluación activa de eventos adversos luego de la vacunación contra la fiebre amarilla en personas de 60 años o más Vaccines Immunother. DO110.4l61/hv.22714.



